Лечение злокачественной опухоли мозга с помощью стволовых клеток
Модифицированные стволовые клетки против агрессивной опухоли мозга
19 мая 2022 года в журнале Nature Communications было опубликовано исследование1 американских ученых о разработке нового метода лечения глиобластом после хирургических вмешательств с помощью стволовых клеток, взятых у здоровых доноров и измененных для атаки опухолевых клеток, специфичных для глиобластом. Эта методика продемонстрировала высокую эффективность на доклинических моделях глиобластомы — 100% мышей прожили более 90 дней после лечения. В будущем данная разработка может полностью заменить постоперационную лучевую- и химиотерапию в качестве более эффективной и безопасной противорецидивной терапии.
Актуальность проблемы
Глиобластома — это наиболее частая и самая злокачественная форма опухолей головного (Grade IV) и спинного мозга с крайне неблагоприятным прогнозом2. Глиобластомы встречаются в 14,7 % случаев всех опухолей ЦНС и в 47,7 % случаев среди злокачественных опухолей головного мозга3.
Глиобластомы трудно поддаются лечению, потому что многие противоопухолевые препараты не могут пройти через ГЭБ. Более того, свыше 90 % глиобластом рецидивируют после стандартного протокола: хирургическое удаление и последующая химио- и лучевая терапия.
Инновационный подход
«Насколько нам известно, это первое исследование, которое распознает рецепторы-мишени на опухолевых клетках до начала терапии и использует инкапсулированную в гель биоразлагаемую терапию на основе модифицированных стволовых клеток после хирургии глиобластом», — сказал Khalid Shah, доктор философии, директор Центра стволовых клеток и трансляционной иммунотерапии (CSTI). «В будущем мы будем применять эту стратегию, чтобы быстро идентифицировать рецепторы-мишени после того, как человек получит диагноз „глиобластома“, а затем вводить терапевтическое средство, инкапсулированное в гель со стволовыми клетками из заранее подготовленного резервуара». Сейчас разберемся, что всё это значит.
Научная проблема
Многие клеточные методы лечения рака основаны на получении материала из собственных стволовых или иммунных клеток пациента. Однако при глиобластомах большинство пациентов оперируют в первую неделю после постановки диагноза из-за быстрого прогрессирования заболевания, что даёт мало времени для разработки терапевтических средств из собственных клеток пациента. Ученые разработали новую методику использования аллогенных стволовых клеток, то есть клеток от здоровых доноров, чтобы лекарство было доступно для введения сразу во время операции. Khalid Shah и его коллеги оценили эффективность воздействия капсул с терапевтическими стволовыми клетки на головной мозг и обнаружили, что капсула из биоразлагаемого гидрогеля успешно справляется с поставленной задачей, не вымываясь спинномозговой жидкостью.
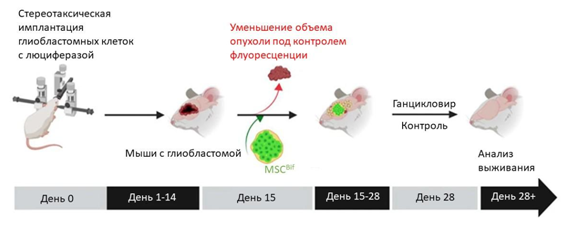
Ученые впервые распознали специальные рецепторы, названные «рецепторами смерти» на циркулирующих опухолевых клетках — или раковых клетках в кровотоке — с использованием генетического биомаркера, обычно экспрессируемого на опухолевых клетках. После распознавания исследователи взяли стволовые клетки из костного мозга здоровых доноров и модифицировали их таким образом, чтобы они высвобождали белки, которые связываются с «рецепторами смерти» и инициировали гибель клеток. Они также встроили защитный механизм в систему стволовых клеток, который позволяет отслеживать стволовые клетки с помощью позитронно-эмиссионной томографии и при активации уничтожать стволовые клетки, тем самым еще больше увеличивая гибель злокачественных клеток. Наконец, команда ученых оценила эффективность терапевтических бифункциональных мезенхимальных стволовых клеток (MSCBif) на животных моделях первичных и рецидивных глиобластом после операции.
Триумф ученых
Результаты оказались поразительными: среднее время жизни мышей, которым проводилось только хирургическое удаление опухоли, составило примерно 55 дней, однако все мыши, которым после операции вводили новое средство, были живы через 90 дней после лечения. Исследователи дополнительно оценили безопасность лечения, проведя несколько экспериментов с использованием различных доз при терапии MSCBif. В ходе этих исследований не было обнаружено признаков токсичности у мышей с опухолями или без таковых.
Обнадеживающие выводы
Результаты данной научной работы открывают путь к клиническим испытаниям I фазы на людях с глиобластомой, перенесших операцию на головном мозге, которые будут проводиться в течение следующих двух лет. Ученые отмечают, что разработанная методика потенциально может быть применима к более широкому спектру солидных опухолей, однако для этого необходимы дальнейшие исследования.
«Помимо значительного успеха данной терапии, наши результаты показывают, что мы можем использовать стволовые клетки здоровых людей для лечения больных раком», — отметил Khalid Shah. «Эта работа закладывает основу для начала создания сконструированного биобанка терапевтических стволовых клеток, нацеленного на различные рецепторы как на опухолевых клетках, так и на иммунных клетках в микроокружении опухоли, которые мы однажды сможем использовать для лечения широкого спектра трудно поддающихся лечению опухолей, таких как глиобластома».
- Bhere, D., Choi, S. H., van de Donk, P., Hope, D., Gortzak, K., Kunnummal, A., ... & Shah, K. (2022). Target receptor identification and subsequent treatment of resected brain tumors with encapsulated and engineered allogeneic stem cells. Nature Communications, 13(1), 1-16.
- Клинические рекомендации Первичные опухоли центральной нервной системы (2020).
- Яковленко Ю.Г. (2019). Глиобластомы: современное состояние проблемы. Медицинский вестник Юга России, (4), 28-35.
Обсудить последние новости со всеми коллегами России вы можете в чатах:
- WhatsApp: https://chat.whatsapp.com/Izj3ZQ7aI36KK8e2dCjcm4
- Telegram: https://tglink.ru/joinchat/GWBPCkkLipQUnTbXrKqzGA
- ВКонтакте: https://vk.me/join/AJQ1dzabQRfHvl5Y2AOVUsgJ






